Este là chất gì? Là một hợp chất hóa học giữ vai trò không thể thiếu trong đời sống sản xuất nhất là trong lĩnh vực công nghiệp. Để biết rõ về khái niệm, công thức, phân loại, tính chất và ứng dụng của este thì quý bạn đọc đừng bỏ lỡ bất kỳ nội dung thông tin nào dưới đây của sieusach.info
Nội dung chính
Este là chất gì?
Este là hợp chất hóa học được hình thành bằng cách thay thế hydro của axit bằng nhóm alkyl hoặc hữu cơ khác. Este là sản phẩm thu được khi thay thế nhóm OH bằng nhóm OR trong axit cacboxylic.

Este là một trong những phần kiến thức quan trọng của Vật Lý 12
Nhà hóa học người Đức Leopold Gmelin đã mang tới thuật ngữ este vào nửa thế kỷ 19. Tên este xuất phát từ rượu mẹ và axit mẹ. Tất cả các este được đặt tên dựa theo cách sử dụng tên IUPAC có thể thống và được hỗ trợ tên cho axit theo hậu tố “-oate”. Công thức hóa học của este hữu cơ đó là R CO2R’, trong đó:
- R: Gốc hidrocacbon của axit
- R’: Gốc Hidrocacbon của ancol
Hiểu một cách đơn giản nhất, este là hợp chất hữu cơ phức tạp, được tạo thành từ sự liên kết giữa axit cacboxylic và ancol. Trong đó, nhóm -OH trong -COOH của axit sẽ thay thế bằng -OR’ của ancol.
Sự hình thành của este
Như thông tin đã cập nhật ở trên, este được hình thành do phản ứng ngưng tụ giữa rượu (R’-OH) và axit cacboxylic (R-COOH), toàn bộ phản ứng này được gọi là quá trình este hóa. Phản ứng ngưng tụ được đặc trưng bởi sự liên kết của hai chất phản ứng để tạo thành sản phẩm cuối cùng lớn hơn về số lượng phân tử và loại bỏ một phần tử nhỏ hơn. Trong các phản ứng este hóa, nước (H2O) là phần tử nhỏ hơn và bị loại bỏ.
R’OH + RCOOH ⇌ RCOOR′ + H2O
Thế nhưng, rượu hữu cơ và axit cacboxylic không phản ứng dễ dàng và khi xảy ra, phản ứng rất thuận nghịch. Vậy nên, một chất xúc tác axit như axit sunfuric thường được thêm vào hỗn hợp chất phản ứng.
Chất xúc tác phục vụ 2 mục đích đó là tăng tốc độ phản ứng và hoạt động giống như chất khử nước. Axit sunfuric tiêu thụ phân tử nước bị loại bỏ, ngăn chặn quá trình thủy phân este mới hình thành. Điều này buộc phải cân bằng phản ứng sang phải, dẫn tới sản lượng sản phẩm lớn hơn. Bên cạnh đó, quá trình este hóa được thực hiện ở nhiệt độ gần như điểm sôi của rượu để tăng tốc độ phản ứng.
Đây không phải là phương pháp duy nhất được áp dụng để sản xuất este. Este còn được tạo ra bằng cách hợp nhất 2 phân tử axit cacboxylic thông qua việc xử lý diazomethane hoặc epoxit, phản ứng với acyl clorua (RCOCI) hoặc với anhidrit axit (R(CO)O(CO)R’) với rượu hoặc anken (CnH2n) với cacbonyl kim loại,…Este cũng có thể được tạo ra từ một este khác bằng việc sử dụng quá trình chuyển hóa.
Công thức cấu tạo este
Estes là sản phẩm được tạo thành khi thay nhóm OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm -OR. Este đơn giản có công thức cấu tạo như sau:
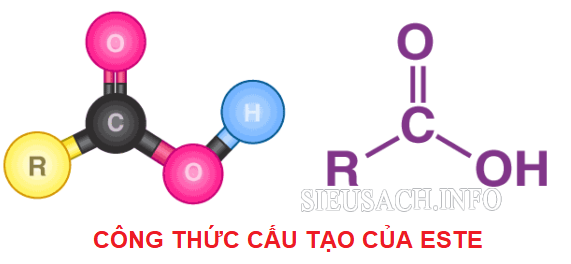
Công thức cấu tạo của este
Este là chất dẫn xuất của axit cacbonxylic. Một số dẫn xuất khác của axit cacboxylic có công thức cấu tạo sau.

Ngoài ra, còn có một số công thức tổng quát của các loại este thường gặp sau:
- Este no, đơn chức, mạch hở: CnH2n+1COOCmH2m+1 hay CxH2xO2 (n ≥ 0; m ≥ 1; x ≥ 2).
- Este đơn chức: CxHyO2 hoặc RCOOR’ (x ≥ 2; y ≥ 4; y chẵn; y ≤ 2x):
- Este của axit đơn chức và Ancol đa chức: (RCOO)xR’.
- Este của axit đa chức và Ancol đơn chức: R(COOR’)x.
- Este của axit đa chức và Ancol đa chức: Rt(COO)xyR’x.
Phân loại este
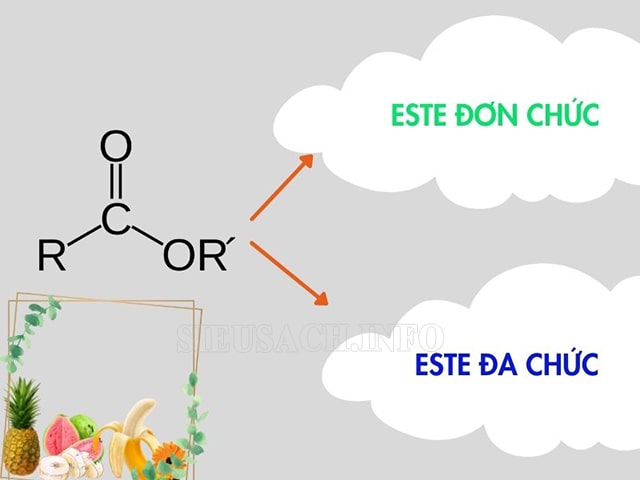
Phân loại este
Dựa vào gốc axit và gốc ancol mà este được chia thành các nhóm chính sau:
Este đơn chức: Là loại este được tạo thành từ acid đơn chức cùng ancol đơn chức. Công thức chung của este đơn chức là RCOOR’, trong đó R là gốc hidrocacbon và R’ là gốc ancol.
Este đa chức
- Este của acid đa chức và ancol đơn chức có công thức cấu tạo chung (RCOO)mR’ với R’ là gốc ancol.
- Este của acid đa chức và ancol đa chức có công thức cấu tạo chung là R(COOR’)n (n ≥ 2; R ≥ 0).
- Este của acid đa chức và ancol đa chức (ít gặp) có dạng chung là Rm(COO)nmR’n. Nếu m=n thì tạo este vòng có dạng R(COO)nR’.
Bên cạnh đó còn có cách phân chia khác đó là este no và este không no dựa vào gốc axit cacboxylic.
Cách gọi tên este đơn giản, chính xác nhất
Danh pháp của este được gọi theo công thức sau:
Tên este = Tên ancol R’ + tên gốc axit (đuôi at)
Đối với este đơn chức R’OH
Tên este = tên gốc hidrocacbon của ancol (yl) + tên gốc hidrocacbon của axit (đổi đuôi ic thành at)
Ví dụ:
- HCOOC2H5: Etyl fomat
- CH3COOC2H5: Etyl axetat
- CH2=CH-COO-CH3: Metyl acrylat
Đối với este đa chức
Với ancol đa chức: Tên este = tên của ancol + tên của gốc axit (đuôi at)
Ví dụ: (C2H5COO)2C2H4: etylenglicol propionat
Với axit đa chức thì tên gọi sẽ được gọi theo tên riêng của từng este
Ví dụ: C3H5(COOC17H35)3: tristearin
Tính chất vật lý của este
Tính chất vật lý của este như sau:
- Các este thường tồn tại ở thể lỏng nhưng với este có phân tử lượng lớn thì sẽ tồn tại ở dạng chất rắn.
- Nhiệt độ sôi của este khá thấp. So với những axit hữu cơ có cùng khối lượng phân tử hay cùng số cacbon thì este có nhiệt độ sôi thấp hơn.
- Este ít tan trong nước, khi so sánh với axit cacboxylic thì độ tan của este trong nước kém hơn do khả năng liên kết hidro giữa các phân este với nước kém hơn.
- Hợp chất este dễ bay hơi, có mùi hương đặc trưng. Điển hình như este isoamyl axetat có mùi chuối chín; etyl propionat có mùi dứa, geranyl axetat có mùi hoa hồng,…
Tính chất hóa học của este

Tính chất hóa học của este
Bên cạnh tính chất vật lý thì bạn cũng cần biết tính chất hóa học của este để biết tránh những sai sót trong quá trình điều chế, ứng dụng. Tính chất hóa học của este như sau:
Phản ứng thủy phân của este
- Trong môi trường axit, phản ứng thủy phân của este là phản ứng thuận nghịch.
Công thức hóa học như sau: RCOOR’ + H2O (H+) ⇔ RCOOH + R’OH
- Trong môi trường kiềm, phản ứng thủy phân của hợp chất este được gọi là phản ứng xà phòng hóa,
Công thức: RCOOR’ + NaOH → RCOONa + R’OH
- Khi thủy phân este của ancol không no trong môi trường axit sẽ tạo ra andehit hoặc xeton.
Công thức như sau: CH3COOCH=CH2 + H2O → CH3COOH + CH3CHO
- Este của phenol khi thủy phân ở trong môi trường NaOH sẽ tạo ra muối phenolat.
Công thức hóa học như sau: CH3COOC6H5 + 2 NaOH → CH3COONa + C6H5ONa + H2O
- Phản ứng khử của este bằng LiAIH4:
Công thức như sau: RCOOR’ → RCH2OH + R’OH (chất xúc tác: nhiệt độ, LiAlH4)
VD: CH3COOC2H5 → CH3CH2OH + C2H5-OH
- Phản ứng đốt cháy este tạo CO2 và H2O
VD: CH3COOC2H5 + 3O2 → 4CO2 + 4H2O
- Phản ứng cộng đối với este không no
- Phản ứng trùng hợp với este không no
nCH2=C(CH3)–COOCH3 → (CH2=C(CH3)–COOCH3) (plexiglass)
- Este của axit fomic có tính chất như một andehit
Phương pháp điều chế este
Để điều chế este thường dùng thì sẽ cho phản ứng este hóa giữa axit cacboxylic và ancol. Đây là phản ứng thuận nghịch xảy ra trong môi trường axit H2SO4đ, nhiệt độ.
R(COOH)x + xR’OH <=> R(COOR’)x + xH2O
yR(COOH)x + xR'(OH)y <=> Ry(COO)xyR’x + xyH2O
xRCOOH + R'(OH)x <=> R'(OOCR)x + xH2O
- Để điều chế este của phenol thì ta cho anhidrit axit hoặc clorua axit tác dụng với phenol:
(C2H5CO)2O + C6H5OH → C2H5COOC6H5 + C2H5COOH
Nếu muốn điều chế este không no thì ta dùng axit cacboxylic phản ứng với ankin tương ứng:
RCOOH + C2H2 → RCOOC2H3 (có nhiệt độ và chất xúc tác)
Ứng dụng của este hiện nay

Este được ứng dụng trong nhiều lĩnh vực khác nhau
Este được sử dụng trong nhiều lĩnh vực trong đời sống khác nhau, cụ thể:
- Tạo mùi hương: Vì este có mùi đặc trưng cùng khả năng giữ mùi tốt nên thường được sử dụng để tạo mùi hương cho các sản phẩm nước hoa, mỹ phẩm,…Đồng thời, còn được dùng làm phụ gia hương liệu trong chế biến thực phẩm.
- Làm dung môi hữu cơ: Hợp chất este tan tốt trong dung môi hữu cơ nên được sử dụng làm dung môi hòa tan, dung môi pha sơn, pha mực,…
- Sử dụng trong dược phẩm: Este đóng vai trò là các chất tiền giúp bảo vệ dược chất chính của thuốc hoặc để tạo dạng bào chế, tăng tính khả dụng cho thuốc.
- …
Cách nhận biết este
- Este của axit fomic có khả năng tham gia vào phản ứng tráng gương
- Este được tạo bởi ancol không bền sẽ bị thủy phân thành andehit hoặc có thể tham gia vào phản ứng tráng gương.
- Este không no sẽ phản ứng và làm mất màu dung dịch brom
- Este tạo bởi glixerol hoặc chất béo khi tham gia thủy phân sẽ tạo ra sản phẩm hòa tan Cu(OH)2.
Với các nội dung thông tin có trong bài viết “Este là chất gì? Công thức, Phân loại, tính chất, ứng dụng cụ thể” hy vọng sẽ giúp ích bạn. Truy cập sieusach.info để cập nhật thêm nhiều thông tin hữu ích khác
Xem thêm:
- [Hoá học]Phản ứng thế là gì? Cho ví dụ và bài tập áp dụng
- Phản ứng xà phòng hóa là gì? Các loại phản ứng xà phòng hóa
- Phản ứng nhiệt nhôm là gì? Hiệu suất phản ứng nhiệt nhôm